+1 Daha
Ribonükleik asit (RNA), fosfodiester bağlarıyla birbirine bağlanmış riboz nükleotitlerinden oluşan yüksek moleküler ağırlıklı bir biyopolimerdir. Her nükleotit, bir riboz şekerine bağlı bir azotlu baz—adenin (A), guanin (G), sitozin (C) veya urasil (U)—içerir. RNA, gen ekspresyonu ve hücresel düzenlemede merkezi bir rol oynar; haberci, yapısal bileşen, düzenleyici ve bazı virüslerde DNA yerine genetik bilgiyi taşıyan bir molekül olarak işlev görür.
Tüm RNA molekülleri, DNA dizilerinin transkriptleri olarak ortaya çıkar; ancak her transkript işlevsel bir rol üstlenmez. Bu nedenle, RNA türlerinin anlamlı bir şekilde sınıflandırılabilmesi için işlevsel RNA'lar ile işlevsiz transkripsiyon yan ürünleri arasında net bir ayrım yapılması gereklidir.
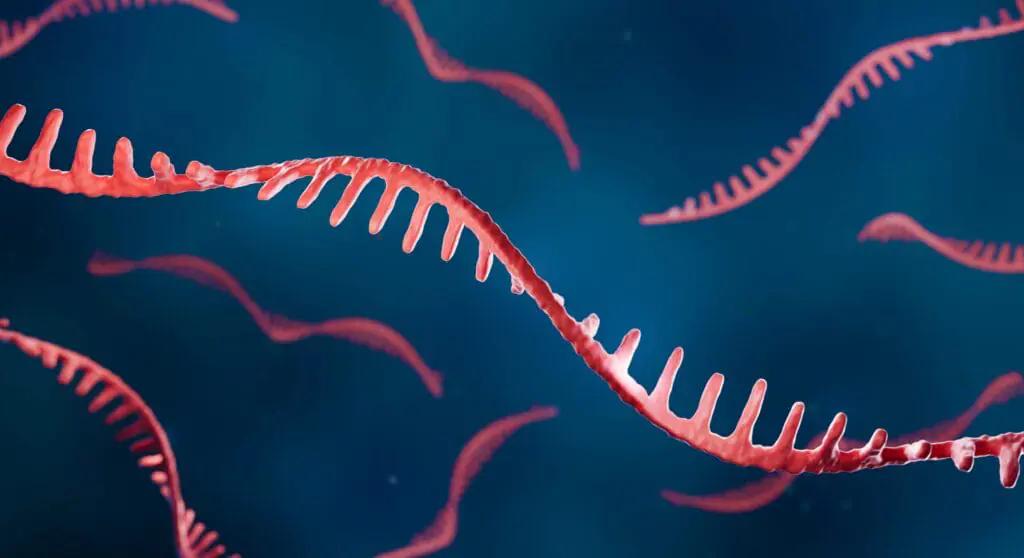
RNA Yapısı( yourgenome)
1961 yılında haberci RNA'nın keşfinden ve 2021 yılında FDA onaylı ilk mRNA aşısının geliştirilmesinden bu yana geçen 60 yıldan fazla sürede, özellikle RNA terapötikleri alanında, RNA araştırmaları dünya çapında kayda değer bir ilerleme ve dönüşüm geçirmiştir. RNA kesilmesi (1977), kendi kendine kesilebilen ribozimler (1982) ve ilk mikroRNA gibi önemli keşifler, klinik uygulamaların önünü açmıştır. Antisens oligonükleotidler (ASO'lar), hedef mRNA'lara özgül olarak bağlanarak gen ekspresyonunu azaltırken; aptamerler, protein hedeflerine yüksek özgüllük ve afinitesiyle bağlanarak antikorlara benzer şekilde davranırlar. RNA bazlı ilaçların en büyük avantajlarından biri, daha önce “ilaçlanamaz” olarak kabul edilen molekülleri, özellikle kodlamayan RNA’ları hedefleyebilmeleridir. Kararsızlık, bağışıklık aktivasyonu ve düşük hücre içi alım gibi zorluklara rağmen, taşıyıcı teknolojilerdeki ilerlemeler bu sınırlamaların üstesinden gelmektedir. Genel olarak RNA terapötikleri; nörolojik, kardiyovasküler, genetik, kanser ve enfeksiyöz hastalıkların tedavisinde küresel düzeyde umut verici araçlar olarak öne çıkmakta; geleneksel ilaç geliştirme yaklaşımlarına göre daha hızlı, daha uygun maliyetli ve uyarlanabilir alternatifler sunmaktadır.
Türkiye'de, RNA bazlı tespit ve transkriptomik analizler alanında son yıllarda kayda değer araştırmalar gerçekleştirilmiştir. Dikkate değer bir örnek, TOBB Ekonomi ve Teknoloji Üniversitesi’nden Dr. Ersin Emre Ören’in ABD’li kurumlarla ortak yürüttüğü çalışmadır. Bu çalışmada, atomik ölçekli elektrotlar kullanılarak E. coli genetik materyali tek molekül düzeyinde tespit edilmiştir. Bu yöntem, DNA/RNA'daki tek nükleotid varyasyonlarının attomolar konsantrasyonlarda tanımlanmasına olanak tanıyarak, yüksek hassasiyetli genetik tanılarda yeni bir yaklaşım sunmaktadır. Ayrıca, 2011–2023 yılları arasında koyunlarda RNA dizileme ve gen ekspresyonu çalışmalarına dair bibliyometrik haritalama, Türkiye’den sınırlı sayıda yayın olduğunu göstermekte, bu alanda bir boşluk ve gelecek potansiyelini vurgulamaktadır. Türk araştırmacılar, küresel bilimsel eğilimlerle uyumlu olarak, aynı zamanda yerel tarım ve biyomedikal ihtiyaçlara hitap edecek şekilde ırka özgü genetik varyantlar, antiparazitik ilaç direnci ve iklimle ilişkili hayvansal özellikler gibi konuları araştırmaya teşvik edilmektedir.
RNA genellikle tek sarmallı bir yapıya sahiptir, ancak kendisiyle eşleşebilen bölgeler içerdiğinden, intramoleküler baz eşleşmesi yoluyla ikincil ve üçüncül yapılar oluşturabilir. Bu yapılar—kabarıklıklar, döngüler ve helezonlar gibi—metilasyon gibi kimyasal modifikasyonlarla stabilize edilir. Yapısal stabilite, RNA’nın işlevi için kritik öneme sahiptir; kararsız RNA’lar genellikle işlevsizdir ve hücresel kalite kontrol mekanizmaları tarafından hızla parçalanır.
Ayrıca, RNA'lar sıklıkla proteinlerle birleşerek ribonükleoprotein komplekslerini (RNP) oluşturur. Bazı durumlarda, RNA bileşeni kendiliğinden katalitik aktivite gösterebilir ve böylece yalnızca proteinlere atfedilen işlevleri üstlenebilir.
Metilasyon ve ikincil yapı, RNA stabilitesine önemli katkılarda bulunan iki kritik özelliktir. mRNA’nın 5′ ucunda yer alan N7-guanozin (m⁷G) metilasyonu, m⁷G kap yapısını oluşturur; bu yapı, RNA’yı 5′-ekzonükleazlara karşı koruyarak genel stabilitesini artırır. Ayrıca bu kap, etkili çeviri ve nükleer çıkışı kolaylaştırır. Bununla birlikte, RNA ikincil yapısı—iç baz eşleşmesiyle oluşan saç tokaları, döngüler ve psödodüğüm yapıları gibi—nükleazlara karşı erişilebilirliği azaltarak yapısal stabilite sağlar. mRNA’lar büyük ölçüde lineer olmasına rağmen, ökaryotlarda nükleotidlerinin yaklaşık %10–15’i bu yerel ikincil yapılara katılır; viral RNA’larda ise bu oran %30–40’ın üzerine çıkabilir. Bu yapısal öğeler, RNA’yı enzimatik parçalanmaya karşı korur ve hücresel proteinlerle olan etkileşimleri düzenleyerek molekülün işlevsel bütünlüğüne ve ömrüne katkı sağlar.
Türkiye’de araştırmacılar, RNA dizileme teknolojisini T-hücreli akut lenfoblastik lösemi (T-ALL) hastalığını incelemek için uygulamıştır. Bu hastalık için hâlen güvenilir prognostik genetik belirteçler ve net bir moleküler sınıflandırma bulunmamaktadır. Jurkat ve Molt-4 hücre hatlarına ek olarak, sağlıklı timosit alt grupları ve T-ALL hastalarına ait kamuya açık veri setleri (GSE48173) kullanılarak gerçekleştirilen çalışmada, karmaşık transkriptomik verilerin analizine uygun bir biyoinformatik iş akışı oluşturulması hedeflenmiştir. Bulgular, dokuya özgü alternatif kesilme olayları, gen ekspresyonu farklılıkları ve önemli genetik varyasyonları ortaya koymuştur. Bu çalışma, özellikle moleküler tanı ve tedavi stratejilerine katkı sağlayacak hesaplamalı yaklaşımların geliştirilmesi yoluyla, Türkiye’nin genomik araştırma kapasitelerindeki ilerlemeyi yansıtmaktadır.
Transkriptomik çalışmalarda gözlenen artan karmaşıklığı düzenlemek amacıyla üst düzey bir sınıflandırma sistemi önerilmiştir. Bu model, biyolojik işlev temelinde üç ana RNA üst sınıfı tanımlar:
Tanımlı ya da gösterilmiş bir işlevi olmayan RNA molekülleridir. Bu grup, arka plan transkripsiyon ürünleri, parçalanma ara ürünleri, kesilme yan ürünleri (örneğin intronlar) ve işlevsiz okumaya devam eden transkriptleri içerir. Kimyasal olarak RNA olsalar da, biyolojik bağlamda RNA olarak kabul edilmezler ve “transkript” olarak adlandırılırlar.
RNA parçalanması, transkripsiyon sonrası gen düzenlemesinde kritik rol oynar. Houseley ve Tollervey'in belirttiği gibi, RNA sentezi ve kararlı düzeyler arasındaki erken karşılaştırmalar, hücrelerin tuttuklarından daha fazla RNA ürettiğini ve aktif RNA parçalanma sistemlerinin varlığını ortaya koymuştur. Aynı zamanda mikroRNA’lar (miRNA’lar) gen ekspresyonu düzenlemesine önemli katkılarda bulunur. Friedman ve arkadaşlarına göre, insan 3′UTR’lerinde korunmuş 45.000’den fazla miRNA hedef bölgesi bulunmaktadır ve insan protein kodlayan genlerinin %60’ından fazlası, miRNA bağlanmasını korumak amacıyla evrimsel baskı altında kalmıştır. Bu bulgular, RNA stabilitesi ve miRNA aracılı baskılanmanın, gen ekspresyonunun temel düzenleme katmanları olduğunu ortaya koymaktadır.
Bu RNA’lar hücrede yapısal, düzenleyici, katalitik veya taşıyıcı roller üstlenir. Örnekler arasında transfer RNA (tRNA), ribozomal RNA (rRNA), küçük nükleer RNA (snRNA), küçük çekirdekçik RNA (snoRNA), mikroRNA (miRNA) ve PIWI ile etkileşen RNA (piRNA) bulunur. Biyolojik aktiviteleri, onları büyüklük veya köken fark etmeksizin işlevsel RNA olarak tanımlar.
Polipeptitlere çevrilebilme özellikleri ile karakterize edilirler. Açık okuma çerçeveleri (ORF’ler) ve düzenleyici öğeler de içerebilen çevrilmeyen bölgeleri (UTR’ler) bulunur. Ribozomlarda protein sentezi için şablon görevi görürler ve hem kodlayıcı hem de düzenleyici işlevleriyle öne çıkarlar.
Türkiye’de, TÜSEB koordinasyonunda yürütülen Ulusal Genom ve Biyoinformatik Projesi kapsamında transkriptomik ve genomik alanlarında önemli gelişmeler kaydedilmektedir. Bu girişim kapsamında, Türkiye Kanser Enstitüsü, “Mesane Kanseri Tedavisinde Kişiselleştirilmiş Tıp Yaklaşımı: Genomik/Transkriptomik Analizler ve Tümör Modellemesi” başlıklı öncü bir çalışma başlatmıştır. Bu proje, mesane kanseri hastalarından elde edilen kapsamlı genomik ve transkriptomik verilerin, klinik ve ilaç direnci bilgileriyle birleştirilerek işlevsel bir genomik kaynak oluşturulmasını amaçlamaktadır. Illumina platformları ile yüksek derinlikte tam genom dizileme (WGS) ve tam transkriptom dizileme (WTS) kullanılan çalışmada, terapötik yanıtları değerlendirmek amacıyla 3B tümör organoid kültürleri de geliştirilmektedir. Bu çaba, Türkiye’de kişiselleştirilmiş onkolojide temel bir adımı temsil etmekte olup, meme kanseri gibi diğer kanser türlerine de genişlemesi planlanmaktadır; böylece yenilikçi tedavi stratejilerinin geliştirilmesine katkı sağlanması ve uluslararası bilimsel iş birliklerinin güçlendirilmesi hedeflenmektedir.
RNA sınıfları arasındaki sınırlar çoğu zaman akışkandır. Örneğin, bazı mRNA’lar, UTR’lerinde kodlamayan düzenleyici öğeler içererek kısmen Sınıf I RNA’larla örtüşür. Tersine, bazı Sınıf I RNA’lar zaman zaman çevrilebilen kısa açık okuma çerçeveleri (ORF’ler) içerir ve bu da onları çift işlevli RNA’lar haline getirir.
Hibrit moleküller de mevcuttur. Örneğin bakteriyel tmRNA, tRNA ve mRNA işlevlerini birleştirir. 5′ ve 3′ uçları kovalent olarak bağlanarak halka oluşturan dairesel RNA’lar (circRNA’lar), miRNA süngeri olarak işlev görebilir veya çeviri şablonu olarak görev alabilir. Ancak, circRNA’ların büyük çoğunluğu, genellikle anormal kesilme yoluyla üretilir, işlevsizdir ve Sınıf 0 transkriptler olarak sınıflandırılır.
Doğal olarak ifade edilen bir dairesel RNA olan ciRS-7, 70’ten fazla korunmuş bağlanma bölgesi içererek miR-7 için güçlü bir sünger görevi görür; miRNA aracılı parçalanmaya dirençlidir ve miR-7 aktivitesini azaltır. ciRS-7 ve miR-7’nin fare beyninde birlikte ifade edilmesi, nöronal dokularda işlevsel bir etkileşime işaret eder. Ayrıca, testise özgü circRNA olan Sry, miR-138 için bir sünger gibi davranır ve bu da circRNA aracılı miRNA düzenlemesinin yaygın bir endojen mekanizma olabileceğini göstermektedir.
ssrA geni, tmRNA’yı kodlar ve tüm dizilenmiş öbakteriyel (eubacterial) genomlarda ve bazı plastid kromozomlarında bulunur. tmRNA molekülleri genellikle 325–400 nükleotid uzunluğundadır, ancak plastitler ve siyanobakterilerde indirgenmiş evrim nedeniyle daha kısa formları da mevcuttur. Yapısal varyantlar, bazı α-proteobakteriler ve siyanobakterilerde de görülür; burada tmRNA iki kovalent olmayan RNA zincirinden oluşur. tmRNA bir öncül olarak transkribe edilir ve olgun formuna RNaz’lar aracılığıyla işlenir. 5′ ucu RNaz P tarafından oluşturulur; 3′ uç olgunlaşması ise, E. coli'de çalışıldığı üzere, RNaz E ve eksonükleaz aktivitesi içerir.
Yüksek ve düşük yumurta verimine sahip tavukların hipotalamus ve hipofiz dokularında yapılan transkriptom analizinde, 4.644 farklı şekilde ifade edilen gen tespit edilmiştir. Düşük yumurta verimine sahip tavuklar, hipotalamo-hipofiz-tiroid (HPT) ekseni genlerinin yukarı regülasyonunu gösterirken, yüksek verimli tavuklar artmış beta-östradiol aktivitesi sergilemiştir. Tiroid hormonu, yüksek verimli tavuklarda gonadotropin mRNA’sını daha fazla baskılarken, östradiol düşük verimlilerde gonadotropin mRNA’sını uyarıp yüksek verimlilerde baskılamıştır. Bu bulgular, yumurta verimi ile ilişkili olarak HPG ekseninin farklı hormonal düzenlemelerini vurgulamaktadır. Bu tür bulgular, Türkiye’de kanatlı hayvan ıslahı ve üreme araştırmalarının ilerletilmesi açısından değerlidir.
Kanser hastalarında tanı anındaki tümör evresi, nüks, ilerleme ve mortalite üzerinde önemli bir etkiye sahiptir. Ancak, birçok kanser türü için erken tanı yöntemleri ya da tarama testleri bulunmamaktadır; bu da mikroRNA tabanlı tanıaraştırmalarını umut verici bir alan haline getirmiştir. MikroRNA’lar, kanser hücrelerine ve dokuya özgü ekspresyon profilleri ve vücut sıvılarında bulunabilirlik gibi biyobelirteçler için uygun özelliklere sahiptir. Ayrıca, taze ya da formalinle fikse dokularda ve vücut sıvılarında kimyasal olarak stabil olmaları, onları daha uzun mRNA’lara ya da uzun kodlamayan RNA’lara kıyasla daha uygun hale getirir. MikroRNA’lar hem sağlıklı hem de kanserli hücreler tarafından salgılandığından, kan, idrar veya dışkı örneklerinde potansiyel tanısal belirteçler olarak özel ekspresyon imzalarının belirlenmesine yönelik çalışmalar yoğunlaşmıştır.
Kanser hücreleri (Sağlık Bakanlığı)
tRNA’lar ve tRNA-türevli fragmanlar (tRF’ler) de hastalıklarla ilişkilidir. tRNA’lar, kaspaz proteinleriyle etkileşerek apoptozu inhibe edebilir; bu mekanizma kanser hücrelerinin hayatta kalmasıyla ilişkilidir. RNA-bağlayıcı proteinleri (RBP’ler) tutarak onları işlevsiz hale getiren tekrar eden RNA dizileri, amyotrofik lateral skleroz (ALS) ve miyotoni distrofi gibi nörolojik hastalıklarda görülür. RBP’lerin mutasyonları ve yanlış düzenlenmeleri birçok insan hastalığına katkı sağlamaktadır.
RNA dizileme ve transkriptomik profil çıkarma konularındaki gelişmeler, MALAT1 gibi tümöre özgü RNA belirteçlerinin keşfini mümkün kılmıştır; bu RNA, kanser metastazı ve hücre proliferasyonu ile ilişkilidir.
MALAT1, gen düzenlemede görev alan korunaklı ve bol bulunan bir uzun kodlamayan RNA’dır. MALAT1 genini eksik olan farelerde gelişimsel bir bozukluk gözlemlenmemesine rağmen, bu RNA akciğer ve çeşitli diğer kanserlerde metastazla ilişkilendirilmiştir. MALAT1’in rolü, kanser türüne ve deneysel modele bağlı olarak değişir ve farklı inaktivasyon yöntemleri farklı etkiler yaratabilir. MALAT1’in kanser ilerlemesindeki işlevini açıklamak için birden fazla mekanizma önerilmiştir.
Brady, K., H. C. Liu, J. A. Hicks, ve diğerleri. “Transcriptome Analysis of the Hypothalamus and Pituitary of Turkey Hens with Low and High Egg Production.” BMC Genomics 21 (2020): 647. https://doi.org/10.1186/s12864-020-07075-y.
Brighton, Katie, and Eliza Small. Addressing RNA Research Challenges. Technology Networks, 18 Ekim 2022. Erişim 19 Temmuz 2025. https://www.technologynetworks.com/biopharma/blog/addressing-rna-research-challenges-366380.
Brosius, Jürgen, and Carsten A. Raabe. “What Is an RNA? A Top Layer for RNA Classification.” RNA Biology 13, no. 2 (2016): 140–144. https://doi.org/10.1080/15476286.2015.1128064.
Duong, Hong-Quan, Minh-Cong Hoang, Thi-Hue Nguyen, Van-Lang Ngo ve Van-Thu Le. “Chapter Six - RNA Therapeutics History and Future Perspectives.” Progress in Molecular Biology and Translational Science, 2024. https://doi.org/10.1016/bs.pmbts.2024.01.004.
Friedman, R. C., K. K. Farh, C. B. Burge ve D. P. Bartel. “Most Mammalian mRNAs Are Conserved Targets of microRNAs.” Genome Research 19, no. 1 (Ocak 2009): 92–105. https://doi.org/10.1101/gr.082701.108.
Hansen, T. B., T. I. Jensen, B. H. Clausen, J. B. Bramsen, B. Finsen, C. K. Damgaard ve J. Kjems. “Natural RNA Circles Function as Efficient microRNA Sponges.” Nature 495, no. 7441 (21 Mart 2013): 384–388. https://doi.org/10.1038/nature11993.
Houseley, J., ve D. Tollervey. “The Many Pathways of RNA Degradation.” Cell 136, no. 4 (20 Şubat 2009): 763–776. https://doi.org/10.1016/j.cell.2009.01.019.
Janssen, Brian D., ve Christopher S. Hayes. “The tmRNA Ribosome Rescue System.” Advances in Protein Chemistry and Structural Biology 86 (2012): 151–191. https://doi.org/10.1016/B978-0-12-386497-0.00005-0.
Kornienko, Igor V., Olga Yu Aramova, Anna A. Tishchenko, Dmitriy V. Rudoy ve Michael Leonidas Chikindas. “RNA Stability: A Review of the Role of Structural Features and Environmental Conditions.” Molecules 29, no. 24 (18 Aralık 2024): 5978. https://doi.org/10.3390/molecules29245978.
Pichler, M., ve G. A. Calin. “MicroRNAs in Cancer: From Developmental Genes in Worms to Their Clinical Application in Patients.” British Journal of Cancer 113 (2015): 569–573. https://doi.org/10.1038/bjc.2015.245.
Sun, Y., ve L. Ma. “New Insights into Long Non-Coding RNA MALAT1 in Cancer and Metastasis.” Cancers (Basel) 11, no. 2 (13 Şubat 2019): 216. https://doi.org/10.3390/cancers11020216.
Turgutlu 6 Nolu Aile Sağlığı Merkezi. “Kanser Nedir?” Genel Sağlık Bilgileri. Erişim 19 Temmuz 2025. http://www.turgutlu6noluasm.com/index.php/saglik-bilgi/genel-saglik-bilgileri/item/258-kanser-nedir.
Türkiye Kanser Enstitüsü (TÜSEB). “TÜSEB Kanser Tedavisinde Kişisel Tıp Yaklaşımıyla Yeni Bir Dönem Başlatıyor.” Türkiye Kanser Enstitüsü, 10 Eylül 2024. Erişim 19 Temmuz 2025. https://tke.tuseb.gov.tr/haberler/tuseb-kanser-tedavisinde-kisisel-tip-yaklasimiyla-yeni-bir-donem-baslatiyor-20240909.
Wellcome Sanger Institute. “What is RNA?” Your Genome. Erişim 19 Temmuz 2025. https://www.yourgenome.org/theme/what-is-rna/.
Henüz Tartışma Girilmemiştir
"RNA (Ribonükleik Asit)" maddesi için tartışma başlatın
Moleküler Yapı
Sınıflandırma ve İşlevsel Hiyerarşi
Sınıf 0 – Transkriptler
Sınıf I – İşlevsel RNA’lar
Sınıf II – Haberci RNA’lar (mRNA’lar)
Yapısal ve İşlevsel Çeşitlilik
İnsan Hastalıklarında RNA
Bu madde yapay zeka desteği ile üretilmiştir.